Диагностика аберраций в генах семейства FGFR у пациентов с метастатическим и местнораспространенным уротелиальным раком
- Семейство генов FGFR
- Аберрации генов семейства FGFR у пациентов с уротелиальным раком
- Методы выявления аберраций генов семейства FGFR при уротелиальном раке
- Программа диагностики:
Семейство генов FGFR
Сигнальный путь FGF/FGFR играет ключевую роль во многих нормальных физиологических процессах, включая эмбриональные, такие как индукция мезодермы, передне-задняя дифференциация, развитие конечностей, индукция и развитие нервной ткани, а в зрелых тканях – ангиогенез, организация кератиноцитов, заживление ран.
FGFR 1-4 – трансмембранные рецепторы с тирозинкиназными внутриклеточными доменами. Гомология между рецепторами составляет от 75% до 51% (наиболее отличающийся – FGFR4).
Гены FGFR 1-4 располагаются в хромосомах 8, 10, 4 и 5 соответственно.
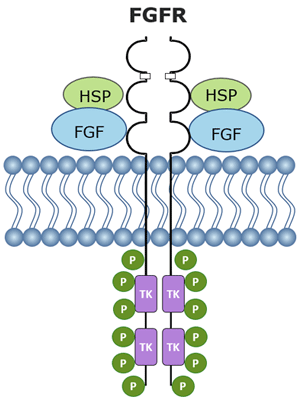
Известно 22 вида лигандов FGF, но только 18 из них достоверно вызывают активацию и димеризацию рецепторов, что приводит к активации нескольких сигнальных путей, активирующих митогенез, ангиогенез, клеточную дифференциацию, выживание, подвижность и инвазию (рис.1) [1,2].
Рисунок 1. Структура и схема активации рецепторов семейства FGFR.
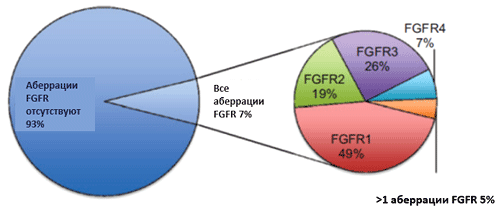
Аберрации генов семейства FGFR чрезвычайно распространены при самых разнообразных злокачественных новообразованиях (рис.2). При анализе почти 5000 опухолей различной локализации исследователями из Центра персонализированного противоопухолевого лечения (Сан-Диего, США) было выявлено, что аберрации в генах FGFR1-4 обнаруживаются в 7% случаев с преобладанием аберраций в гене FGFR1 (рис.3). При этом самым частым видом нарушений является амплификация (66%), реже встречаются мутации (26%), еще реже – транслокации (около 8%) [3].
Рисунок 2. Частота встречаемости аберраций генов семейства FGFR у пациентов с опухолями различной локализации [2].
Рисунок 3. Относительная частота нарушений в генах FGFR1-4 при злокачественных новообразованиях [3].
Аберрации генов семейства FGFR у пациентов с уротелиальным раком
Особенностью уротелиального рака (УР) является достаточно высокая частота встречаемости нарушений в генах семейства FGFR и довольно ограниченный спектр этих аберраций. Так, общая их частота при УР составляет около 33%, при этом чаще всего встречаются активирующие мутации FGFR3 (15%), а именно: S249C, R248C, Y373C, G370C и K650M. Три мутации FGFR3: R248C, S249C и Y373C составляют >85% из всех обнаруженных однонуклеотидных нарушений. Существенно реже встречаются перестройки генов FGFR (около 6% от всех выявленных нарушений), причем подавляющее большинство этих транслокаций происходят также с участием гена FGFR3 (FGFR3–TACC3, FGFR3–BAIAP2L1) [4].
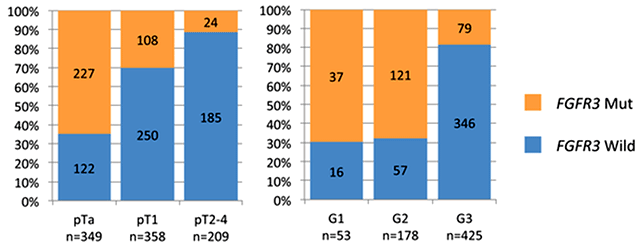
Нарушения в генах семейства FGFR при УР ассоциированы с определенными клинико-морфологическими и биологическими особенностями опухоли. Встречаемость мутаций в гене FGFR3 снижается с увеличением степени злокачественности и стадии опухоли (рис.4). Таким образом, наиболее часто эти аберрации могут быть обнаружены в поверхностных опухолях низкой степени злокачественности на ранних стадиях (до 70% в рТ1аG1), а в опухолях рT2-4G3 их частота их снижается до 12-18%. В то же время, согласно Консенсусной молекулярной классификации мышечно-инвазивного УР 2019 г., мутации FGFR3 ассоциированы с папиллярным подтипом люминального типа инвазивного УР, названного так по схожести экспрессионых генетических характеристик с люминальными раками молочной железы. В этом подтипе инвазивного УР частота мутаций FGFR3 варьирует от 33% до 44%, а общее количество нарушений в этом гене (мутаций, амплификаций и транслокаций) может составлять более 50% [5,6]. Данное кажущееся несоответствие связано с тем, что подавляющее большинство поверхностных УР относится к люминальному папиллярному подтипу, соответственно, люминальный папиллярный инвазивный рак является следствием прогрессии раннего люминального рака, сохраняя все его генетические характеристики.
Рисунок 4. Различия в частоте мутаций в гене FGFR3 в зависимости от распространенности и степени злокачественности опухоли [5].
Методы выявления аберраций генов семейства FGFR при уротелиальном раке
Для выявления нарушений в генах семейства FGFR3 могут использоваться следующие методы: для детекции мутаций – ПЦР и секвенирование (в том числе – высокопроизводительное), для детекции перестроек – ПЦР, FISH и высокопроизводительное секвенирование. Каждый из методов имеет свои преимущества и недостатки, отраженные в таблице 1.
Таблица 1. Сравнительная характеристика методов исследования.
| Метод | Преимущества | Недостатки |
|---|---|---|
| ПЦР (ДНК или РНК) | Широко распространенная, относительно дешевая методика, выполняется во всех лабораториях | Могут быть выявлены только входящие в набор реагентов нарушения |
| Высокопроизводительное секвенирование (ДНК и РНК) | Могут быть выявлены все возможные нарушения в исследуемых генах | Сложная дорогая методика, может выполняться только высококвалифицированным персоналом в ограниченном количестве лабораторий |
| FISH (тканевая методика) | Достаточно распространенная методика, выполняется во многих лабораториях | Могут быть выявлены перестройки и амплификация гена, не выявляются мутации, довольно дорогая методика |
В настоящее время оптимальным методом признается обратно-транскриптазная цепная реакция, основанная на исследовании РНК и позволяющая выявлять наиболее распространенные аберрации в генах FGFR2 и FGFR3 – точечные мутации и перестройки. Предпочтительным набором считается коммерческий набор компании QIAGEN therascreen FGFR RGQ RT-PCR Kit, валидированный в международных клинических исследованиях (в т.ч. BLC2001) [7] и детектирующий наиболее частые нарушения в генах FGFR3 и FGFR2, которые встречаются при УР (таблица 2). Набор позволяет выявлять более 95% всех аберраций исследуемых генов, характерных для УР [8].
Таблица 2. Генетические нарушения, выявляемые набором therascreen FGFR RGQ RT-PCR Kit (QIAGEN) [8].
| Панель исследуемых аберраций |
|---|
| Точечные мутации FGFR3: R248C (экзон 7) S249C (экзон 7) G370C (экзон 10) Y373C (экзон 10) |
| Транслокации FGFR3: FGFR3:BAIAP2L1 FGFR3:TACC3v1 FGFR3:TACC3v3 |
| Транслокации FGFR2: FGFR2:CASP7 FGFR2:BICC1 |
Программа диагностики
Кому, когда, зачем и как проводить тестирование?
Тестирование целесообразно проводить пациентам с местнораспространенным и метастатическим уротелиальным раком сразу по выставлении этого диагноза, до начала химиотерапии первой линии. Обнаруженные аберрации в дальнейшем могут стать причиной назначения эффективной таргетной терапии. Известен ряд препаратов, ингибирующих FGFR и таким образом оказывающих противоопухолевое действие, в том числе селективные пан-FGFR-ингибиторы, находящиеся в активной клинической разработке. В настоящее время ожидается регистрация их применения во второй и последующих линиях терапии.
Как?
01.10.2021 г. открыта новая опция диагностической программы «Совершенствование молекулярно-генетической диагностики в Российской Федерации с целью повышения эффективности противоопухолевого лечения» по выявлению аберраций в генах FGFR у пациентов с метастатическим и местнораспространенным уротелиальным раком. Врач, проводящий на территории РФ наблюдение и лечение пациента с уротелиальным раком, теперь может заказать молекулярное тестирование биологического материала через сайт CANCERGENOME.ru, зарегистрировавшись в Программе.
Доставка и тестирование биологического материала, а также предоставление результатов тестирования осуществляются бесплатно для лечебного учреждения, врача и пациента.
Консультацию по оформлению заказа на молекулярное тестирование можно получить по телефону горячей линии программы CANCERGENOME:
Какой материал должен направляться на тестирование?
На тестирование направляется биопсийный/операционный материал первичной опухоли или метастаза в виде парафинового блока и соответствующего гистологического стекла.
Образец должен быть обязательно просмотрен патоморфологом для оценки количества содержащейся опухолевой ткани. Оптимально образец должен содержать 50% и более опухолевой ткани, опционально – не менее 20% опухолевой ткани. К исследованию допускаются архивные образцы возрастом не старше 5 лет. Более старые образцы могут быть приготовлены с существенными нарушениями и подвергнуться существенному окислению с разрушением нуклеиновых кислот.
 Благодарим ООО «Джонсон & Джонсон» за спонсорскую поддержку проекта диагностики аберраций в генах семейства FGFR
Благодарим ООО «Джонсон & Джонсон» за спонсорскую поддержку проекта диагностики аберраций в генах семейства FGFR
Список литературы:
- Dai S, et al. Fibroblast Growth Factor Receptors (FGFRs): Structures and Small Molecule Inhibitors. Cells. 2019, 8, 614.
- Krook M, et al. Fibroblast growth factor receptors in cancer: genetic alterations, diagnostics, therapeutic targets and mechanisms of resistance. Br J Cancer. 2021 Mar; 124(5): 880-892.
- Helsten T, et al. The FGFR Landscape in Cancer: Analysis of 4,853 Tumors by Next-Generation Sequencing Clin Cancer Res. 2016 Jan 1; 22(1): 259-67.
- Al-Obaidy KI, Cheng L. Fibroblast growth factor receptor (FGFR) gene: pathogenesis and treatment implications in urothelial carcinoma of the bladder. J Clin Pathol. 2021; 74: 491-495.
- Neuzillet Y, et al. A Meta-Analysis of the Relationship between FGFR3 and TP53 Mutations in Bladder Cancer. PLoS ONE. 2012; 7(12): e48993.
- Kamoun, et al. A Consensus Molecular Classification of Muscle-invasive Bladder Cancer. Eur Urol. 2020 April; 77(4): 420-433.
- Loriot Y, et al. Erdafitinib in Locally Advanced or Metastatic Urothelial Carcinoma. N Engl J Med. 2019; 381: 338-48.
- QIAGEN FGFR CE-IVD Handbook, Nov-2019 (доступ 29.10.2021).
- Совершенствование системы молекулярно-генетической диагностики онкологических заболеваний в Российской Федерации. www.cancergenome.ru.
Войти
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
в программе
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.