Транслокации с участием гена ALK
- Тестирование на наличие транслокации гена ALK
- Функции ALK в норме и при развитии злокачественных опухолей
- Зачем определять статус транслокации ALK?
- Кому нужно проводить тестирование?
- Методы диагностики
Тестирование на наличие транслокации гена ALK
Тест на наличие транслокации гена ALK показан больным распространенным немелкоклеточным раком легкого с отрицательным статусом EGFR мутации для отбора пациентов на терапию препаратами алектиниб, кризотиниб или церитиниб.
Транслокация гена ALK – это внутрихромосомная перестройка (парацентрическая инверсия) короткого плеча 2-й хромосомы, ведущая к образованию химерного онкогена EML4/ ALK примерно в 95% случаев. Еще в 5% случаев транслокация возникает с участием других генов, представляя из себя, как правило, истинную реципрокную транслокацию. Иногда образование типичного химерного онкогена сопровождается частичной делецией 3’ части гена ALK, биологическое значение этого феномена пока до конца не изучено.
Понимание роли транслокации гена ALK в развитии немелкоклеточного рака легкого (НМРЛ) стало одним из важнейших шагов в дальнейшей расшифровке генома этого заболевания и расширении возможностей персонализации его лечения.
Функции ALK в норме и при развитии злокачественных опухолей
ALK является рецепторной тирозинкиназой из семейства инсулинзависимых рецепторов. В норме протеин ALK активно экспрессируется в нервной ткани только во время эмбриогенеза, регулируя пролиферацию нейронов.
Как и у любой тирозинкиназы, основной функцией этого рецептора является передача сигнала. Основными сигнальными путями, задействованными в передаче, являются пути PI3K/ERK и RAS/MAPK, то есть те же, что участвуют в передаче сигнала EGFR.
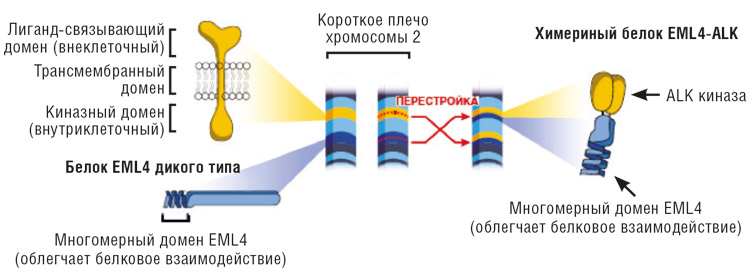
Активация ALK при образовании химерного гена EML4-ALK (рис.1).
Транслокация EML4-ALK ведет к активации киназ
Рисунок 1. Формирование транслокации EML4-ALK.
Таким образом, ALK попадает под влияние регулирующих последовательностей EML4 и переходит в активное состояние, становится независимым от своих лигандов и передает сигнал, постоянно нарушая нормальную дифференцировку и апоптоз клетки.
Зачем определять статус транслокации ALK?
Обнаружение транслокации EML4-ALK при немелкоклеточном раке легкого принципиально для проведения терапии таргетными препаратами алектиниб, кризотиниб или церитиниб, зарегистрированными ингибиторами тирозинкиназы ALK в первой линии.
Кому нужно проводить тестирование?
Частота встречаемости транслокаций с участием ALK при немелкоклеточном раке легких по данным разных авторов колеблется от 3% до 13% в зависимости от особенностей выборки.
Прослеживается четкая ассоциация транслокации EML4-ALK со следующими характеристиками опухоли и больного:
- Гистологически – аденокарцинома, более 94%.
- Отсутствие конкурирующих мутаций (EGFR, KRAS, BRAF, PIK3CA).
- Некурящие, более 67%.
Тем не менее, следует помнить, что все клинические рекомендации (включая рекомендации RUSSCO) рекомендуют направлять на исследование всех пациентов с распространенным неплоскоклеточным НМРЛ, вне зависимости от пола, национальности и статуса курения. Ограничение по этим параметрам может привести к потере до 50% пациентов с транслокацией.
Методы диагностики
Первым методом, использованным во всех регистрационных исследованиях, стал метод флюоресцентной гибридизации in situ (FISH), в настоящее время остающийся «золотым стандартом» прямого определения транслокаций с участием гена ALK. Наиболее широко используется рекомендованная FDA методика с использованием пробы LSI ALK Break Apart Rearrangement Probe (Abbott Molecular, США).
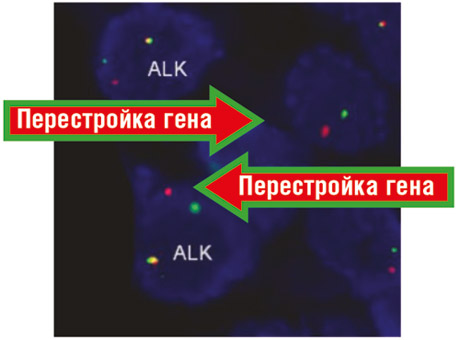
Проба представляет собой два флюоресцентных зонда, конъюгированных с красителями разного цвета (оранжевым и зеленым) и комплементарных расположенным рядом последовательностям гена ALK. В норме обе пробы гибридизуются рядом и при просмотре в флюоресцентный микроскоп формируют сигнал желтого цвета или видны как расположенные вплотную два сигнала красного и зеленого цвета. При перестройке гена и перемещении одной из его последовательности сигналы расходятся и видны как лежащие раздельно (рис. 2).
Рисунок 2. Перестройка гена при немелкоклеточном раке легкого (аденокарцинома). Данные ГБ №62 г.Москва.
Использование этого набора обладает высокой чувствительностью и специфичностью (до 98-100%) и позволяет правильно определить ALK-статус опухоли более чем в 90% случаев.
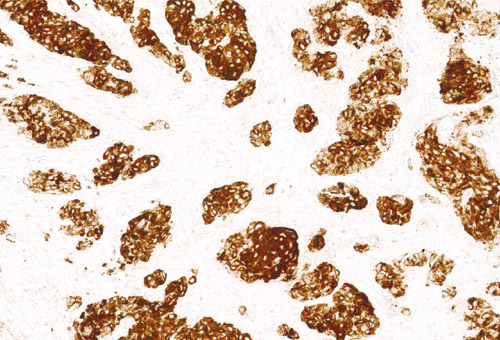
В настоящее время именно ИГХ-метод широко используется для первичного скрининга образцов НМРЛ. Однако наличие артефактов и 5-10% сомнительных случаев требует использования альтернативных методов (как правило, FISH) для точной детекции транслокации (рис. 3).
Рисунок 3. ИГХ-позитивное окрашивание образца НМРЛ.
Другим, также теоретически универсальным методом, является иммуногистохимическое исследование (ИГХ), позволяющее выявить высокую экспрессию химерного протеина в цитоплазме опухолевых клеток.
На текущий момент зарегистрированы и одобрены FDA два коммерчески доступных антитела, все более широко использующиеся для определения продукта перестроек гена ALK при НМРЛ. Из них общепризнанный приоритет имеет антитело D3F4, используемое с системой детекции и амплификации VENTANA (Roche Diagnostic) и адаптированное для приборов VENTANA.
Третьим методом, используемым в диагностике реаранжировок ALK, является обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР). Метод обладает высочайшей чувствительностью, позволяет работать с образцами, содержащими крайне низкое количество опухолевых клеток, способен сразу идентифицировать тип перестройки.
Тем не менее, ОТ-ПЦР обладает несколькими весьма существенными недостатками. Во-первых, метод очень требователен к качеству РНК, выделенной из образца, в особенности – из фиксированного в формалине и залитого в парафин. Во-вторых, с помощью ОТ-ПЦР возможно выявить только те типы перестройки гена ALK, к которым подобраны специфические праймеры, что требует мультиплицирования исследования и существенных временных затрат.
Очень интересным подходом является метод сравнительной экзонной экспрессии, позволяющий увидеть транслокации с помощью изучения разности экспрессии 3’ и 5’ концов гена ALK. Но и этот метод требует высочайшей квалификации специалистов и может выполняться далеко не в любой лаборатории.
Пока все методы детекции транслокаций ALK на основе ПЦР не зарегистрированы в РФ.
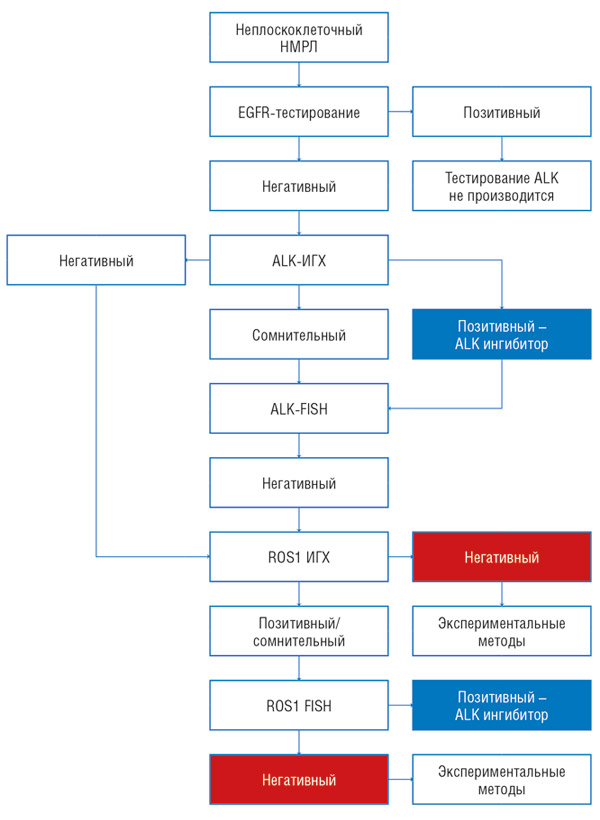
В рамках Программы алгоритм диагностики по выявлению транслокации ALK и ROS1 у пациентов с немелкоклеточным раком легкого представлен на рис. 4.
Рисунок 4. Алгоритм тестирования.
Список литературы:
- Soda M, Choi YL, Enomoto M, et al. Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer. Nature. 2007; 448(7153): 561-566.
- Iwahara, T, Fujimoto J, Wen D, et al. Molecular characterization of ALK, a receptor tyrosine kinase expressed specifically in the nervous system. Oncogene 1997, 14: 439-449.
- Stoica, GE, Kuo A, Aigner A, et al. Identification of anaplastic lymphoma kinase as a receptor for the growth factor pleiotrophin. J. Biol. Chem. 2001; 276: 16772-16779.
- Bai RY, Ouyang T, Miething C, et al. Nucleophosmin-anaplastic lymphoma kinase associated with anaplastic large-cell lymphoma activates the phosphatidylinositol 3-kinase/Akt antiapoptotic signaling pathway. Blood 2000; 96: 4319-4327.
- Marzec M, Kasprzycka M, Liu X, et al. Oncogenic tyrosine kinase NPM/ALK induces activation of the rapamycin-sensitive mTOR signaling pathway. Oncogene 2007; 26: 5606-5614.
- Medves S, Demoulin JB. Tyrosine kinase gene fusions in cancer: translating mechanisms into targeted therapies. J. Cell. Mol. Med. 2012; 16(2): 237-248.
- Crystal AS, Show AT. Variants on a Theme: A Biomarker of Crizotinib Response in ALKPositive Non–Small Cell Lung Cancer. Clin Cancer Res 2012; 18(17): 4479-81.
- Horn L, Pao W. EML4-ALK: Honing In on a New Target in Non–Small-Cell Lung Cancer. J Clin Oncol 2009, 27(26): 4232-4235.
- Camidge DR, et al. Activity and safety of crizotinib in patients with ALK-positive nonsmall-cell lung cancer: updated results from a phase 1 study. Lancet Oncol 2012; 13: 1011-1019.
- Kim, et al. Updated Results of a Global Phase II Study with Crizotinib in Advanced ALK-positive Non-small Cell Lung Cancer. ESMO 2012; Abstract 1230PD.
- Food and Drug Administration. Summary review (application number: 202570Orig1s000). Food and Drug Administration 2011, Silver Spring.
- Camidge DR, Hirsch FR, Varella-Garcia M, Franklin WA. Finding ALK-positive lung cancer: what are we really looking for? J Thorac Oncol. 2011; 6(3); P.411-3.
- Meno-Kenudson M, Chirieac LR, Law K, et al. A novel, highly sensitive antibody allows for the routine detection of ALK-rearranged lung adenocarcinomas by standard immunohistochemistry. Clin Cancer Res. 2010; Vol.1; No.16(5; P.1561-71.
- Sanders HR, Li HR, Bruey JM, et al. Exon scanning by reverse transcriptase-polymerase chain reaction for detection of known and novel EML4-ALK fusion variants in non-small cell lung cancer. Cancer Genet. 2011; Vol.204; No.1; P.45-52.
- Lindeman NI, Cagle PT, Beasley MB, Chitale DA, Dacic S, Giaccone G, Jenkins RB, Kwiatkowski DJ, Saldivar JS, Squire J, Thunnissen E, Ladanyi M. Molecular Testing Guideline for Selection of Lung CancerPatients for EGFR and ALK Tyrosine Kinase Inhibitors. Guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. J Mol Diagn. 2013 Jul; 15(4): 415-53. doi: 10.1016/j.jmoldx.2013.03.001. Epub 2013 Apr 4. P.21-24.
- Acquaviva J, Wong R, Charest A. The multifaceted roles of the receptor tyrosine kinase ROS in development and cancer. Biochim Biophys Acta 2009; 1795: 37-52.
- Charest A, Lane K, McMahon K, et al. Fusion of FIG to the receptor tyrosine kinase ROS in a glioblastoma with an interstitial del(6)(q21q21). Genes Chromosomes Cancer 2003; 37: 58-71.
- Rikova K, Guo A, Zeng Q, et al. Global survey of phosphotyrosine signaling identifies oncogenic kinases in lung cancer. Cell 2007; 131: 1190-203.
- Gu TL, Deng X, Huang F, et al. Survey of t yrosine kinase signaling revea ls ROS kinase fusions in human cholangiocarcinoma. PLoS One 2011; 6(1): e15640.
- Davies KD, Doebele RC. Molecular pathways: ROS1 fusion proteins in cancer. Clin Cancer Res 2013; 19: 4040-5.
- Gainor JF, Shaw AT. Novel targets in non-small cell lung cancer: ROS1 and RET fusions. Oncologist 2013; 18: 865-75.
Войти
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
в программе
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.